ماهي اغلب العناصر الموجودة على يسار الجدول الدوري في الكيمياء
ماهي اغلب العناصر الموجودة على يسار الجدول الدوري في الكيمياء، حيث يعتبر معظم العناصر الموجودة على يسار الجدول الدوري هي تلك العناصر التي لها مجموعة من الخصائص التي تجعلها فريدة داخل جدول العناصر حيث تكررت هذه العبارة كثيرًا وازداد التحقيق في العناصر مؤخرًا عدة مرات على يسار الجدول الدوري.
محتويات المقال
تعرف على الجدول الدوري للعناصر
- لعب الجدول الدوري للعناصر الكيميائية دورًا لا يمكن إنكاره في تتبع العناصر التي أدت إلى العديد من الاكتشافات العلمية، وهو جدول مستطيل جمعه الكيميائي الروسي مندليف عام 1869م.
- والذي يجمع العناصر الطبيعية أو المواد ذات الطبيعة الكيميائية وفقًا لتكوينها الذري وترتيب الإلكترونات والشحنات بالترتيب العرضي للخاصية والدورة والعدد الذري لكل عنصر من اليسار إلى اليمين بترتيب تنازلي، من أعلى إلى أسفل.
- يحتوي الجدول الدوري على ست مجموعات بالإضافة إلى الأرقام المخصصة لها، لذلك إذا قلنا على سبيل المثال إن العناصر والمواد في المجموعة السابعة عشرة تمثل الهالوجينات، بينما تمثل المواد والعناصر في المجموعة رقم ثمانية عشر ما يسمى الغازات النبيلة.
- بالإضافة إلى ذلك، تتميز هذه العناصر بالتطابق في خصائص معينة بحيث يتم توزيعها وفقًا الدورة، لأن عناصر خط عرضي واحد تحتوي على عنصر واحد، بينما تشتمل الفئة أو المجموعة على خط عمودي.
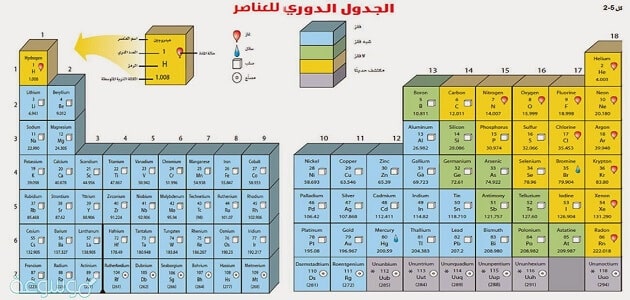
- ويتكون الجدول الدوري من سبعة أسطر كل صف يسمى فترة، ومعظم العناصر الموجودة على يسار الجدول الدوري عبارة عن فئة معادن، بينما تحتل اللافلزات الفئات اليمنى.
شاهد أيضًا: تجربتي مع اليود المشع وتاثيره على الاخرين
ما هي مكونات الجدول الدوري للعناصر؟
حيث يتكون هيكل الجدول الدوري من صفوف عرضية تبدأ من اليسار ونهاية إلى اليمين وتسمى دورات، ويتم ترتيب الأعمدة الرأسية بترتيب تنازلي من أعلى إلى أسفل وتسمى مجموعات، بحيث تكون العناصر ذات الأنشطة الكيميائية يتم تنظيمهم هناك.
يوجد هناك مجموعة من البيانات والتحليلات في الجدول الدوري للعناصر يتم مشاركتها من قبل المجموعات والجلسات، ومن أهم هذه البيانات:
- اسم المادة: تتضمن معظم الجدول الدوري يحمل اسم العنصر أو المادة مع الرمز المصاحب.
- رمز المادة: يمثل الرمز اختصارًا مكونًا من حرف أو حرفين لاتينيين، على سبيل المثال يُشار إلى رمز الهليوم بالرمز المكون من “HE”، بينما يتكون رمز عنصر الكربون على سبيل المثال، من الحرف اللاتيني “C”.
- العدد الذري: هو عدد البروتونات التي تتكون منها الذرة، وهي وحدة واحدة من وحدات العنصر، وهي تختلف من عنصر لآخر وهي أيضًا تختلف عن الإلكترونات.
- الكتلة الذرية: يتم التعامل معها على أنها متوسط كتلة العنصر، بالنسبة لبقية أمثاله.
تعرف على تصنيف العناصر حسب خصائصها الكيميائية
تتكون عناصر الجدول الدوري من نوعين:
- النوع الأول: يمثل العناصر الموجودة على يسار الجدول، لأن معظم العناصر الموجودة على يسار الجدول الدوري هي عناصر معدنية تحدث بشكل طبيعي، ويتم تمثيلها في العناصر المتسلسلة للجدول الدوري من رقم 1 إلى رقم 98.
- النوع الثاني: يمثل المركب أو العناصر التي تصنعها المعامل، ويشكل مجموعة اللافلزات وأشباه الفلزات، ويتضمن العناصر المترتب عليها في الجدول الدوري من رقم 99 إلى رقم 118.
ما أهمية استخدام الجدول الدوري للعناصر؟
- الجدول الدوري للعناصر ذو أهمية كبيرة لأنه يستخدم في التصنيف الدولي للعناصر حسب مسارات العدد الذري.
- كما يستخدم في إجراء التجارب بناءً على خصائص العناصر الذرية.
- يستخدم الجدول الدوري للعناصر كمصدر أساسي لأي شخص مهتم بالكيمياء والعلوم الطبيعية والعلوم الطبية وما إلى ذلك.
- من خلال معرفة الجدول الدوري ودراسة وتحديد جميع خصائص العناصر وتحديدها، يمكن للكيميائيين وعلماء الطبيعة إجراء تجاربهم ومعادلاتهم بطريقة صحية ومثالية وبمعايير محددة تعتمد على العلم والتخطيط الدقيق.
قد يهمك: سيليكات الصوديوم السائلة
تعرف على أغلب العناصر الموجودة على يسار الجدول الدوري
يعلم الكيميائيون أن معظم العناصر الموجودة على يسار الجدول الدوري هي عناصر معدنية فلزية تحدث بشكل طبيعي، والتي إذا قمنا بتضمين العناصر المعدنية وغير المعدنية، تعتبر الخريطة الكيميائية الرئيسية وفقًا لجدول مندليف للعناصر التي من خلالها يشتق الكيميائيون قوانينهم ومركباتهم واكتشافاتهم العلمية والكيميائية.
- يتم تقديم الجدول الدوري للعناصر وفقًا لمندليف والعناصر التي تكتمل بعده في شكل أربعة مجالات على شكل مستطيلات أو مستويات شبه مسطحة تتعلق بملء المسارات الذرية المختلفة.
- ومعظم العناصر الموجودة على يسار الجدول الدوري من بين تلك العناصر التي لها خصائص تجعلها فريدة من نوعها بين العناصر الأخرى فيما يتعلق بالخصائص والخصائص المختلفة.
- توافر وتنوع الأماكن التي تمتلئ فيها الكرة الأرضية بهذه المواد المعدنية الطبيعية مثل الحديد والمغنيسيوم.
- تختلف معادلات المعادن في القلويات مع الأبعاد الأساسية مثل الصوديوم والبوتاسيوم، وهناك تربة قلوية مثل الكالسيوم، أو المعادن الأولية والتحويلية عندما تتحد مع الأكسجين.
- معظم العناصر الموجودة على يسار الجدول الدوري قوية جدًا وقوية جدًا في التركيب.
- تتميز العناصر المعدنية أيضًا بخصائص المرونة والليونة، على الرغم من صلابتها.
- تتميز العناصر المعدنية أيضًا بأنها قادرة على توصيل الطاقة الكهربائية.
- كما أنه يتميز باللمعان والإشراق والتلميع إذا كان خالياً من الشوائب والأتربة الممزوجة به.
- الذوبان عند الوصول إلى نقطة الانصهار والتي عند الوصول إلى هذه النقطة تخضع للتبخر والنقصان.
- وجميع العناصر الأربعة والعشرون التي تمثلها المعادن الانتقالية تحتاج إلى درجة كبيرة من الحرارة لتصل إلى الذوبان باستثناء الزئبق الذي يذوب في درجة الحرارة العادية.
ما تصنيف العناصر في الجدول الدوري؟
بفضل الجدول الدوري للعناصر، يمكن تصنيف العناصر التي تتكون منها على النحو التالي:
الفلزات القلوية
- تمثل الفلزات القلوية المواد والعناصر في المجموعة الأولى من الجدول.
- وتتوافق خصائص العناصر الموجودة على يسار الجدول الدوري مع كثافتها المنخفضة مقارنة بالعناصر الطبيعية الأخرى.
- بالإضافة إلى ذلك، تتميز العناصر المعدنية بتفاعلها القوي مع المواد الأخرى.
- مما يحولها إلى مركبات طبيعية إذا تداخلت مع عناصر أخرى.
الفلزات القلوية الترابية
- تمثل عناصر الفلزات القلوية الترابية مواد المجموعة الثانية في الجدول الدوري للعناصر.
- وتتميز ببريقها وقوتها العالية وقدرتها على الانحناء وتقبل الانحناء أيضًا والتمدد مثل الحديد والنحاس.
المعادن الأساسية
- وهي مادة قادرة على نقل التيار الكهربائي والحرارة وتتميز بكثافتها وخفتها ومن أمثلة المعادن الأساسية: الألومنيوم والثاليوم.
المعادن الانتقالية
- تشتمل هذه المعادن المتحولة أو الانتقالية على خطوات الأكسدة.
- حيث إنها تتضمن مستويات طاقة غير أساسية أو غيرها من المفاهيم غير المملوءة بالإلكترونات.
- وقد تكون متاحة في شكل نقي ولامع، مثل الذهب والفضة وقد تكون متوفر بشكل غامق وغير مضيء.
تابع معنا: كبريتيد الصوديوم واستخداماته
تعرف على خصائص العناصر الفلزية
جميع العناصر المكونة للأيونات الموجبة تسمى الإلكترونات الخاسرة في التفاعلات الكيميائية مع المعادن، لأن المعادن عناصر موصلة للكهرباء ذات طاقات تأين منخفضة نسبيًا وتتميز بتألقها وصلابتها، وللمعادن العديد من الخصائص الفيزيائية والكيميائية وهي:
- الحالة: لأن معظم المعادن عبارة عن مواد صلبة في درجة حرارة الغرفة باستثناء الزئبق السائل عند درجة حرارة الغرفة.
- البريق: تتمتع المعادن بجودة انعكاس الضوء على سطحها ويمكن صقلها مثل الذهب والفضة والنحاس.
- القابلية للتطرق: تتمتع المعادن بالقدرة على تحمل الطرق ويمكن تحويلها إلى صفائح رقيقة تسمى رقائق معدنية.
- الليونة: المعادن لديها ليونة عالية جِدًّا.
- الصلابة: جميع المعادن صلبة ما عدا الصوديوم والبوتاسيوم.
- التكافؤ: تحتوي المعادن بشكل عام على 1 إلى 3 إلكترونات في الغلاف الخارجي لذراتها.
- التوصيل: المعادن موصلات جيدة لاحتوائها على إلكترونات حرة، حيث أن الفضة والنحاس هما أفضل موصلين للحرارة والكهرباء.
- الكثافة: المعادن عالية الكثافة وثقيلة للغاية مع وجود الإيريديوم والأوزميوم أعلى كثافة بين العناصر.
- الانصهار والغليان: حيث تحتوي المعادن على نقاط انصهار وغليان عالية، ويكون للتنجستن أعلى نقطة انصهار وغليان بين العناصر.
وهكذا قد وضحنا لكم في هذا المقال المبسط ما هي أغلب العناصر الموجودة على يسار الجدول الدوري في الكيمياء وتعرفنا على تصنيف العناصر الفلزية وحسب خصائصها الكيميائية، ونتمنى أن نكون قد أجبنا على جميع أسئلتكم ونشكركم على حسن استماعكم إلينا، دمتم في رعاية الله.